Dołącz do newslettera — pierwszy zakup 5% taniej!
Zapisując się do newslettera, wyrażasz zgodę na otrzymywanie informacji handlowych drogą elektroniczną oraz akceptujesz politykę prywatności.
Odbiór jest obecnie niemożliwy
Darmowa dostawa od 50 zł!
Dostawa: 2–5 dni roboczych
Opcje dostawy: Paczkomat InPost, Kurier InPost, Dostawa weekendowa – 30 zł
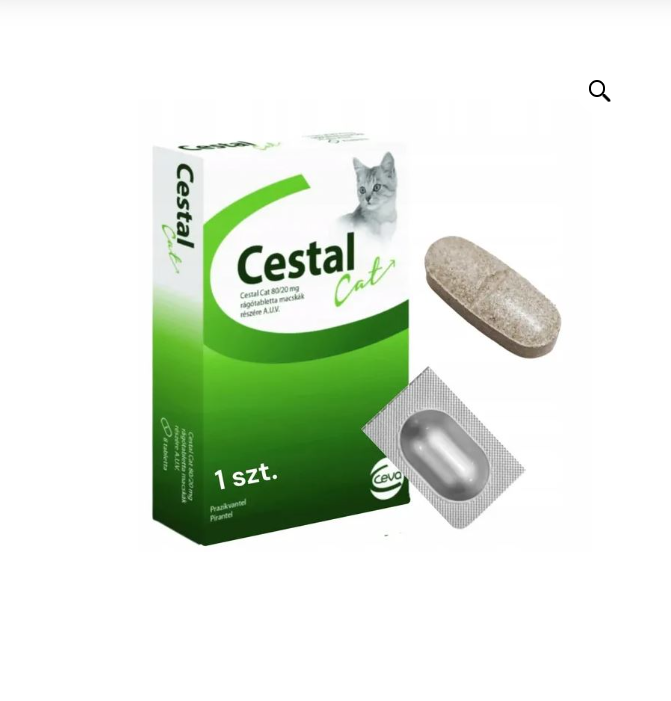
Cestal Cat tabletki na odrobaczenie dla kota 80/20mg - 1 tabletka
Sprzedawane w blistrach oryginalnych od producenta + ulotka, na każdej tabletce znajduje się nazwa produktu, data ważności oraz skład
1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
Cestal Cat 80/20 mg tabletki do rozgryzania i żucia dla kotów
Cestal Cat 80/20 mg chewable tablets for cats (BG, CY, HU, EE, LV, LT, NL, RO, SK, CZ)
Helmex Cat 80/20 mg chewable tablets for cats (FR, IE, UK)
2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Każda tabletka zawiera:
Substancje czynne:
Prazykwantel 20 mg
Pyrantel 80 mg (co odpowiada 230 mg pyrantelu embonianu)
Wykaz wszystkich substancji pomocniczych, patrz punkt 6.1.
3. POSTAĆ FARMACEUTYCZNA
Tabletka do rozgryzania i żucia
Żółtawo - brązowawa, owalna tabletka z linią podziału.
Tabletki można podzielić na dwie równe części.
4. SZCZEGÓŁOWE DANE KLINICZNE
4.1 Docelowe gatunki zwierząt
Koty
4.2 Wskazania lecznicze dla poszczególnych docelowych gatunków zwierząt
Leczenie mieszanych inwazji tasiemców i obleńców u kotów, powodowanych przez następujące
pasożyty:
- glisty: Toxocara cati, Toxascaris leonina (formy dojrzałe i późne niedojrzałe)
- tęgoryjce: Ancylostoma tubaeforme,
- tasiemce: Echinococcus multilocularis, Hydatigena (Taenia) taeniaeformis, Dipylidium caninum
(formy dojrzałe i niedojrzałe), Joyeuxiella spp.
4.3 Przeciwwskazania
Nie stosować w przypadkach nadwrażliwości na substancje czynne lub na dowolną substancję
pomocniczą. Nie stosować u kociąt poniżej 6 tygodnia życia. Nie stosować jednocześnie z produktami
zawierającymi piperazynę. Patrz punkt 4.7.
4.4 Specjalne ostrzeżenia dla każdego z docelowych gatunków zwierząt
Pchły są żywicielami pośrednimi jednego z powszechnie występujących tasiemców - Dipylidium
caninum. Inwazja tasiemców będzie nawracała, jeśli nie zostanie przeprowadzone zwalczanie
żywicieli pośrednich, takich jak pchły i myszy.
Częste i wielokrotne stosowanie leków przeciwpasożytniczych jednej klasy może prowadzić do
uodparniania się pasożytów na leki przeciwpasożytnicze danej klasy.
4.5 Specjalne środki ostrożności dotyczące stosowania
Specjalne środki ostrożności dotyczące stosowania u zwierząt
3
Ponieważ tabletki są smakowe aromatyzowane należy je przechowywać w miejscu niedostępnym dla
zwierząt. Zwierzęta w złej kondycji lub silnie zarobaczone, co może objawiać się występowaniem
takich objawów jak biegunka, wymioty, obecność pasożytów w kale, wymiocinach, pogorszenie
wyglądu sierści, powinny być zbadane przez lekarza weterynarii przed podaniem produktu.
W przypadku kotów poważnie osłabionych lub w przypadku silnej inwazji stosować jedynie po
dokonaniu przez lekarza weterynarii oceny bilansu korzyści/ryzyka wynikającego ze stosowania
produktu.
Specjalne środki ostrożności dla osób podających produkt leczniczy weterynaryjny zwierzętom
Z uwagi na względy higieniczne, osoby podające tabletki kotom bezpośrednio lub przez dodanie do
kociej karmy, powinny potem umyć ręce.
Po przypadkowym połknięciu, należy niezwłocznie zwrócić się o pomoc lekarską oraz przedstawić
lekarzowi ulotkę informacyjną lub opakowanie.
Echinokokoza stanowi zagrożenie dla zdrowia ludzi. Ponieważ echinokokoza jest chorobą podlegającą
obowiązkowi zgłoszenia do Światowej Organizacji na Rzecz Zdrowia Zwierząt (OIE), w celu
uzyskania informacji dotyczących odpowiednich zasad leczenia, jego kontynuacji i zapewnienia
bezpieczeństwa ludzi, należy skontaktować się z kompetentnymi organami.
4.6 Działania niepożądane (częstotliwość i stopień nasilenia)
W bardzo rzadkich przypadkach (mniej niż 1 na 10000 leczonych zwierząt, włączając pojedyncze
raporty) mogą wystąpić łagodne i przemijające zaburzenia układu pokarmowego, takie jak nadmierne
ślinienie i/lub wymioty oraz łagodne i przemijające zaburzenia neurologiczne, takie jak ataksja.
4.7. Stosowanie w ciąży, laktacji lub w okresie nieśności
Nie stosować w czasie ciąży. Może być stosowany w czasie laktacji.
4.8 Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji
Nie stosować jednocześnie z produktami zawierającymi piperazynę.
4.9 Dawkowanie i droga(i) podawania
Dawkowanie
Zalecana dawka to: 20 mg pyrantelu (co odpowiada 57,5 mg pyrantelu embonianu) i 5 mg/kg
prazykwantelu. Odpowiada to 1 tabletce na 4 kg m. c.
Masa ciała (kg) Liczba tabletek
≥1,0 - ≤2,0 ½
>2,0 - ≤4,0 1
>4,0 - ≤6,0 1 ½
>6,0 - ≤8,0 2
Podawanie i czas trwania leczenia
Pojedyncze podanie doustne. Tabletkę do rozgryzania i żucia należy podać zwierzęciu bezpośrednio,
ale jeśli to konieczne, można ją podać w pokarmie.
W przypadku inwazji obleńców, zwłaszcza u młodych zwierząt, nie można spodziewać się całkowitej
eliminacji, a jednocześnie ryzyko zachorowania u ludzi pozostaje.
W badaniu przeprowadzonym na 30 kotach dobrowolne spożycie notowano w 83% przypadków.
Żadne ograniczenie dostępu do pokarmu nie jest wymagane ani przed, ani po podaniu produktu. W
celu zapewnienia podania właściwej dawki, masa ciała zwierzęcia powinna być określona
najdokładniej jak to tylko możliwe.
Należy zasięgnąć porady lekarza weterynarii co do konieczności i częstości powtarzania leczenia.
4
4.10 Przedawkowanie (objawy, sposób postępowania przy udzielaniu natychmiastowej pomocy,
odtrutki), jeśli konieczne
Objawy przedawkowania nie występują po podaniu dawki do 5 razy większej od zalecanej. Po
podaniu dawek wyższych niż 5-krotność zalecanej obserwowano objawy nietolerancji, takie jak
wymioty.
4.11 Okres(-y) karencji
Nie dotyczy
5. WŁAŚCIWOŚCI FARMAKOLOGICZNE
Grupa farmakoterapeutyczna: produkty przeciwpasożytnicze, pochodne chinolonów i substancje
pokrewne, połączenia prazykwantelu
Kod ATC vet: QP52AA51
5.1 Właściwości farmakodynamiczne
Prazykwantel jest bardzo szybko wchłaniany i rozprowadzany po ciele pasożyta. Zarówno badania
prowadzone in vivo jak i in vitro wykazały, że prazykwantel powoduje ciężkie uszkodzenie powłok
pasożyta, prowadzące do skurczu i porażenia. Dochodzi do niemal natychmiastowego skurczu
tężcowego mięśniówki pasożyta i szybkiej wakuolizacji syncytialnego tegumentu. Ten gwałtowny
skurcz został wyjaśniony przez zmiany w przepływie dwuwartościowych kationów, w szczególności
wapnia.
Pyrantel działa jak agonista cholinergiczny. Mechanizm jego działania polega na pobudzeniu
receptorów cholinergicznych nikotynowych pasożyta, indukcji spastycznego porażenia, co pozwala,
dzięki ruchom perystaltycznym, na wydalanie pasożyta z układu pokarmowego.
5.2 Właściwości farmakokinetyczne
Prazykwantel jest szybko wchłaniany, metabolizowany i dystrybuowany w ciele. Po podaniu
doustnym kotom maksymalne stężenia w osoczu osiągane były po około 2 godzinach. Prazykwantel
jest metabolizowany w wątrobie. Jest on całkowicie wydalany, głównie w postaci metabolitów w
moczu, w ciągu 48 godzin po podaniu.
Pyrantel wchłania się w niewielkim stopniu, więc oczekuje się, że duża część podanej dawki pozostaje
w przewodzie pokarmowym, w którym wywiera swój efekt terapeutyczny. Jest wydalany w znaczniej
mierze w postaci niezmienionej z kałem.
6. DANE FARMACEUTYCZNE
6.1 Wykaz substancji pomocniczych
Cetylu palmitynian
Laktoza jednowodna
Skrobia żelowana
Karboksymetyloskrobia sodowa (typ A)
Drożdże suszone
Aromat wątroby, proszek
Magnezu stearynian
6.2 Główne niezgodności farmaceutyczne
5
Nie dotyczy
6.3 Okres ważności
Okres ważności produktu leczniczego weterynaryjnego zapakowanego do sprzedaży: 3 lata.
Okres ważności podzielonych (przepołowionych) tabletek po otwarciu blistra: 2 dni.
6.4 Specjalne środki ostrożności podczas przechowywania
Brak specjalnych środków ostrożności dotyczących przechowywania. Podzielone tabletki należy
zużyć przy kolejnym podaniu, nie później niż po 48 godzinach. W celu przechowania
niewykorzystanej połówki tabletki, należy ją umieścić z powrotem w otwartym blistrze lub blistrze
miękkim oraz w pudełku i przechowywać w bezpiecznym miejscu niedostępnym dla dzieci.
6.5 Rodzaj i skład opakowania bezpośredniego
Produkt jest pakowany albo w blister składający się z kompozytu folii aluminiowej i ze zgrzewanej
folii aluminiowej albo w blistry miękkie wykonane z wielowarstwowego laminatu z folii
Aluminium/Polietylen.
• Pudełko zawierające 1 blister z 2 tabletkami (2 tabletki)
• Pudełko zawierające 2 blistry z 2 tabletkami (4 tabletki)
• Pudełko zawierające 52 blistry z 2 tabletkami (104 tabletki)
• Pudełko zawierające 1 blister z 8 tabletkami (8 tabletek)
• Pudełko zawierające 3 blistry z 8 tabletkami (24 tabletki)
• Pudełko zawierające 6 blistrów z 8 tabletkami (48 tabletek)
• Pudełko zawierające 13 blistrów z 8 tabletkami (104 tabletki)
• Pudełko zawierające 5 blistrów miękkich z 2 tabletkami (10 tabletek)
• Pudełko zawierające 25 blistrów miękkich z 2 tabletkami (50 tabletek)
Niektóre wielkości opakowań mogą nie być dostępne w obrocie.
6.6 Specjalne środki ostrożności dotyczące usuwania niezużytego produktu leczniczego
weterynaryjnego lub pochodzących z niego odpadów
Niewykorzystany produkt leczniczy weterynaryjny lub jego odpady należy usunąć w sposób zgodny z
obowiązującymi przepisami.
7. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO
Ceva Animal Health Polska Sp. z o.o.
ul. Okrzei 1A, 03-715 Warszawa, Polska
8. NUMER(-Y) POZWOLENIA NA DOPUSZCZENIE DO OBROTU
2849/19
9. DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU
/ DATA PRZEDŁUŻENIA POZWOLENIA
Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: 15/02/2019
6
10. DATA OSTATNIEJ AKTUALIZACJI TEKSTU CHARAKTERYSTYKI PRODUKTU
LECZNICZEGO WETERYNARYJNEGO
20/04/2020
ZAKAZ WYTWARZANIA, IMPORTU, POSIADANIA, SPRZEDAŻY, DOSTAWY I/LUB
STOSOWANIA
Nie dotyczy